Samenvatting van de
belangrijkste gegevens
ANATOMIE
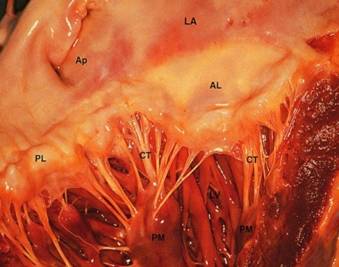
 Het
mitralisklepsysteem (figuur 1.) bestaat uit vier delen en vormt de poort tussen
linker atrium en ventrikel. In een functioneel samenspel met de twee voornoemden
vormen annulus, twee klepbladen (figuur 2), chordae tendineae en
papillairspieren samen een complex dat bepalend is voor de sufficiëntie van de
gehele mitralisklep1,2.
Het
mitralisklepsysteem (figuur 1.) bestaat uit vier delen en vormt de poort tussen
linker atrium en ventrikel. In een functioneel samenspel met de twee voornoemden
vormen annulus, twee klepbladen (figuur 2), chordae tendineae en
papillairspieren samen een complex dat bepalend is voor de sufficiëntie van de
gehele mitralisklep1,2.
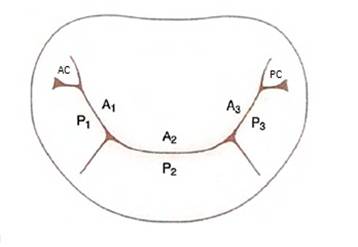

HISTOLOGIE
Histologisch gezien bestaan de klepbladen uit vier bindweefsellagen. Gaande van
de atriale naar de ventriculaire kant: atrialis, spongiosa, fibrosa en
ventricularis. Het is vooral op dit niveau waar zich de pathogenese van
mitralisklepprolaps afspeelt, meer bepaald de toestand van het collageen
(verhoogd type III en minder type I en V)3.
CYTOGENETICA
Cytogenetica is de studie van het chromosoom. Moleculaire genetica heeft
betrekking op de studie van het genetisch materiaal op het niveau van de
individuele nucleotidebasen die het DNA vormen. Dit kan onderzocht worden met
onder andere fluoro in situ hybridisatie (FISH) waarbij de hybridisatie van een
DNA probe aan de complementaire streng wordt gevisualiseerd met behulp van een
fluorescerend reagens. Zo kan dan een specifieke sequentie worden opgespoord.
Een andere methode hiervoor is de vergelijkende genoomhybridisatie (CGH) die
vergelijkbaar is met FISH maar met het verschil dat het test-DNA niet met een
kloon wordt vergeleken maar met een referentie-DNA, met als voordeel dat de
test-cel niet gekweekt hoeft te worden, maar met als nadeel dat translocaties en
inversies niet gedetecteerd kunnen worden. Wanneer de sequentie is geweten kan
men van daaruit proberen om te mappen en linkage te zoeken. Er kunnen moleculair
genetische tests gedaan worden in het kader van diagnostiek, carrierdetectie,
presymptomatische diagnostiek en prenatale diagnostiek. Hierbij wordt vooral
gebruik gemaakt van kwantitatieve fluorescentie PCR, of voor specifieke mutaties
van Southern blotting en gentracking4.
DIAGNOSTIEK
Voor prenatale diagnostiek zijn een aantal mogelijkheden, met het daarbij
behorende risico voor de ongeboren vrucht. Het is belangrijk de patiënt goed te
informeren over deze risico’s en in samenspraak een weloverwogen keuze te maken.
Chorion villus sampling (C. V. S.)
Deze test wordt uitgevoerd op 11 a 12 weken zwangerschap. Bij deze procedure
worden een aantal cellen weggenomen van de ontwikkelende placenta. Deze cellen
zijn geschikt voor chromosoom, DNA en biochemische tests. Het risico op miskraam
na chorion villus sampling ligt tussen de 1 op 20 en 1 op 100. Het resultaat van
de test is normaal gesproken beschikbaar binnen 3 a 10 dagen.
Amniocentese
Deze test wordt gewoonlijk uitgevoerd op ongeveer 16 weken. Een kleine
hoeveelheid van het vruchtwater wordt verwijderd. Hierin bevinden zich huid- en
blaascellen van de foetus. Voordat geschikt DNA kan worden verkregen, moeten de
totale cellen groeien in een laboratorium. Het resultaat zal daarom langer duren
dan bij de vlokkentest. Het risico op miskraam na amniocentese is tussen de 1 op
100 en 1 op 150.
Foetale bloed sampling
Deze test is meer specialistisch en wordt gewoonlijk uitgevoerd op 18 tot 22
weken. Een kleine hoeveelheid foetaal bloed wordt genomen uit de navelstreng of
een klein bloedvat in het foetale abdomen. Het risico op miskraam na foetale
bloed sampling is ongeveer 1 op 100. Het risico op miskraam is hoger wanneer de
test wordt uitgevoerd voor niet genetische redenen zoals resusincompatibiliteit4,
5.
Prenatale echografie
Dit is een niet invasief onderzoek om een beeld te geven van de inhoud van de
uterus. Het wordt routinematig gebruikt om de ontwikkeling van de foetus te
volgen in de vroege zwangerschap en om te kijken naar structurele cardiale
abnormaliteiten vanaf 20 weken.
Wanneer een specifiek risico bestaat dat een foetus aangedaan is door een
genetische aandoening die structurele abnormaliteiten betreft, kunnen door een
ervaren echografist gedetailleerde echo's worden gemaakt tijdens verschillende
stadia in de zwangerschap. De foetus moet voldoende ontwikkeld zijn en defecten
kunnen vaak pas worden uitgesloten na 20 weken zwangerschap4, 5.
Echografie
De gouden standaard voor diagnose van mitralisklepprolaps is op dit moment
tweedimensionale TTE of TEE, die een crosssectionele anatomie van verschillende
componenten van het klepblad leveren. Een vierkamer doorsnede verkregen uit een
apicaal vierkameraanzicht of nul graden doorsnede van midoesofagale TEE "snijdt"
door A2L en P2L. Een apicaal of parasternaal lange as beeld door TTE en een
equivalent lange as beeld door TEE (ongeveer 130 graden) levert een doorsnede
door A2M en P2M. De metingen van de klepbladen ter hoogte van A2 en P2 worden
doorgaans verkregen uit deze doorsnede en komen overeen met de chirurgische
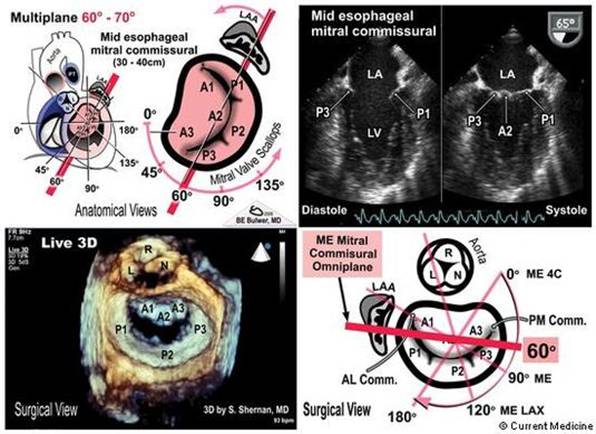

"hoogte" van de klepbladen door directe meting. En extra beeld dat klinisch
bruikbare informatie geeft is het TEE 60 graden beeld (figuur 3). Dit beeld
toont in het algemeen P3, P1 en de vrije hoek van het anterieure klepblad A3, A2
en A1 tijdens systole terwijl het anterieure klepblad zich uit het vlak beweegt
tijdens diastole. In dit beeld is P2 niet zichtbaar tenzij het prolabeert. De
commissurale schelpen zijn niet zichtbaar op deze doorsnede. Een transgastrisch
korte as beeld levert de extra anatomische details van alle segmenten van de
twee klepbladen. Volgens de huidige echografische criteria wordt
mitralisklepprolaps gedefinieerd als een systolische opwaartse verplaatsing van
de mitralisklepbladen van meer dan 2 mm. Bij klassieke mitralisklepprolaps is de
maximale dikte van de klepbladen meer dan 5 mm, dit in tegenstelling tot de niet
klassieke mitralisklepprolaps2, 6.
MITRALISKLEPPROLAPS
Mitralisklepprolaps (MVP) is een aandoening waarbij de klep tijdens systole
uitpuilt in het linker atrium en kent veel verschillende benamingen (systolic
click-murmur syndroom, Barlow’s syndroom, floppy-klep syndroom en billowing
mitral leaflet syndrome).
Ziektes waarbij mitralisklepprolaps kan voorkomen zijn6:
- Sikkelcelanemie
- Bindweefselaandoeningen: Marfan (75% heeft MVP)7, Ehlers-Danlos,
osteogenesis imperfecta en pseudoxanthoma elasticum.
- Neuromusculaire aandoeningen: X-gebonden musculaire dystrofie en myotone
dystrofie.
- SLE en polycystische nierziekten
- Acute reumatische koorts, ischemisch hartlijden en cardiomyopathie en bij 20%
van de patiënten met een ostium secundum ASD.
ETIOLOGIE8
De ziekte van Barlow en fibroelastische deficiëntie zijn de twee dominante
vormen van degeneratieve mitralisklepziekte. (tabel 1.)
Degeneratieve mitralisklepziekte refereert naar een spectrum van aandoeningen
waarbij morfologische veranderingen in het bindweefsel van de mitralisklep
structurele laesies veroorzaken, die normale functie van het mitralisapparaat
verhinderen. Degeneratieve laesies zoals chordale elongatie, chordale ruptuur,
klepbladweefseluitzettingen, en annulaire dilatatie resulteren in
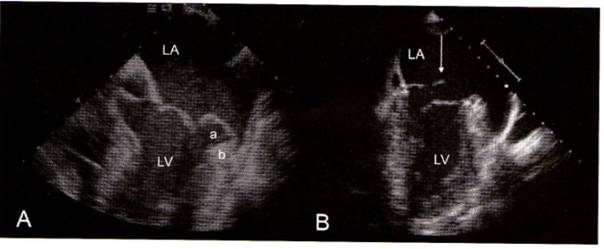
mitralisklepregurgitatie te wijten aan prolaps van het klepblad. In figuur 4
zijn de echografische verschillen te zien.
|
|
Ziekte van Barlow |
Fibroelastische deficiëntie |
|
Pathologie |
Myxoïdinfiltratie |
Verstoorde aanmaak van bindweefsel |
|
Typische leeftijd |
Jong
(meestal <60 jaar) |
Oud
(meestal >60 jaar) |
|
Duur
van gekende mitralisklepziekte |
Enkele jaren tot decaden |
Maanden |
|
Lange
voorgeschiedenis van hartgeruis |
Gewoonlijk |
Nee |
|
Familiale voorgeschiedenis |
Soms |
Nee |
|
Kenmerken van Marfan |
Soms |
Nee |
|
Auscultatie |
Midsystolische click en laatsystolisch geruis |
Holosystolisch geruis |
|
Echo |
Bulkende, fladderende klepbladen, multisegmentele prolaps |
Dunne
klepbladen, prolaps van een enkel segment, geruptureerde chordae |
|
Chirurgische laesies |
Overmatig weefsel, verdikte en/of lange klepbladen, chordale verdikking
of verdunning, chordale elongatie of ruptuur, atrialisatie van
klepbladen, fusie, fibrose of calcificatie van de chordae,
papillairspiercalcificatie, annuluscalcificatie |
Dunne
klepbladen, verdikking en overmatig weefsel (indien aanwezig)
gelimiteerd tot het prolaberende segment, ruptuur van chordae |
|
Klepherstel |
Complex |
Minder complex |
Tabel 1. De verschillen tussen de ziekte van Barlow en fibroelastische
deficiëntie

DIFFERENTIATIE8-12
Cardiologen verwijzen gemakkelijk asymptomatische patiënten met ernstige
mitralisklepregurgitatie8 door naar een chirurg. Een goede
differentiatie van het degeneratieve ziekteproces zou een kritische stap bij het
doorverwijzen moeten zijn. De etiologie en resulterende laesies zijn namelijk
bepalend voor de gebruikte hersteltechniek. Wanneer bijvoorbeeld de
echocardiografie een ernstige ziekte van Barlow toont met een prolaps van beide
klepbladen op meerdere segmenten met annulaire calcificatie, betekent dit dat er
een posterieure klepbladresectie, een ‘sliding’ klepbladplastie, een annulaire
decalcificatie, een chordale transfer of substitutie, een
papillairspierverplaatsing en een grote annuloplastie nodig zijn voor een
succesvol herstel. Dit is vooral belangrijk voor chirurgen die minimaal
invasieve technieken aanbieden, omdat jonge patiënten die zulke technieken
zoeken vaak asymptomatische patiënten met de ziekte van Barlow zijn. Omdat bij
fibroelastische deficiëntie de laesies minder uitgesproken zijn is de ingreep
minder complex.
Voor de duurzaamheid van de reparatie geldt als belangrijk aspect dat een
residuele regurgitatie minimaal moet zijn. Om dit te bekomen is het van belang
dat een patiënt op het juiste moment geopereerd wordt. Opereren bij iemand
zonder klachten is vaak zinvol. Als men wacht tot uitgesproken symptomen
aanwezig zijn, neemt de kans op een succesvolle ingreep af.
Hoewel het herstel van degeneratieve mitraliskleppen reeds 30 jaar wordt gedaan,
blijft de outcome op lange termijn slecht gedefinieerd door gebrek aan gegevens
over de differentiatie tussen de twee voornoemde vormen . Hoewel beschikbare
data aangeven dat patiënten met een prolaps van de twee klepbladen een hogere
kans hebben op recidiverende middelmatige tot ernstige mitralisklepregurgitatie
en heroperatie, kan men vanuit deze gegevens niet differentiëren volgens
etiologie. Differentiatie van degeneratieve ziekte is in de toekomst van
kritisch belang voor de opheldering van zaken als duurzaamheid en resultaten van
de mitralisklepreparatie. De mitralisklepreparatie heeft wel de voorkeur boven
een klepvervanging.
PREVALENTIE13
In 1948 werd een grote populatiestudie gedaan die in 1971 werd hervat met de
verwanten van het originele cohort. In deze studie werden M-mode
echocardiografische bevindingen van mitralisklepprolaps gemeld bij 264 van de
4967 individuen. De prevalentie was 2,5% bij mannen en 7,6% bij vrouwen. De
relatie tussen leeftijd en prevalentie van mitralisklepprolaps bleek een
omgekeerde U-vormige curve met de laagste prevalentie (0,3%) bij kinderen, de
hoogste prevalentie bij adolescente vrouwen (15%), gevolgd door een verdere
reductie bij volwassenen (tot 1,8% bij onderzoekspersonen van 80 jaar en ouder).
Een leeftijdsafhankelijke uiting van mitralisklepprolaps bleek uit verscheidene
andere studies gebaseerd op M-mode echocardiografie. Bij een van die studies
bestond bij ongeveer 6% van de neonaten een echocardiografisch bewijs voor
mitralisklepprolaps bij een nog relatief onderontwikkeld linker ventrikel. De
incidentie van mitralisklepprolaps in de late kindertijd en adolescentie was
rond de 1%. Bij een familiestudie bleek 46% van de eerstegraads verwanten boven
de 20 jaar een echocardiografische mitralisklepprolaps te hebben, terwijl
slechts 16% beneden die leeftijd was aangedaan.
Een van de meest interessante en consistente bevindingen ten aanzien van
mitralisklepprolaps is de correlatie met de asthenische lichaamshabitus. Als de
anorexiapatiënten in gewicht toenamen, tot 80% van hun normaal lichaamsgewicht,
verdween het echocardiografische bewijs voor mitralisklepprolaps. Volgens de
klep-ventrikel-disproportietheorie is mitralisklepprolaps het resultaat van
overmatig mitralisklep weefsel of van een inadequate afmeting van het linker
ventrikel. De afmeting van het linker ventrikel bleek gereduceerd te zijn bij
patiënten met anorexia nervosa. Mitralisklepprolaps blijkt een rol te spelen bij
cardiale aritmie zoals voorkamerfibrillatie, die veelvuldig worden gevonden bij
deze patiënten14.
|
prevalentiecijfers op basis van verschillende studies |
|
|
Mitralisklepprolaps15,16 |
264/4967 |
|
|
|
mannen |
2,5% |
|
|
|
vrouwen |
7,6% |
|
|
|
|
|
|
|
|
|
op leeftijd |
|
|
studie 115,16 |
|
studie 215-17 |
|
|
kinderen |
0,3% |
vrouwen 20-29jaar |
17% |
|
adolescente vrouwen |
15% |
vrouwen 80+ |
1,4% |
|
80+ |
1,8% |
mannen overall |
2-4% |
|
|
|
|
|
|
|
lichaamsgewicht |
|
|
studie 315.16 |
studie 418 |
|
vrouwen BMI<15 |
25% |
anorexia
nervosa |
32% |
|
mannen BMI<15 |
29% |
patiënten |
|
| |
|
|
|
|
Tabel 2. Prevalentiecijfers op basis van verschillende studies
KLINIEK19
De auscultatoire bevindingen zijn een midsystolische click en/of een laat
systolisch geruis.
De anamnese van asymptomatische mitralisklepprolaps is zeer variabel.
Complicaties als hartfalen, mitralisklepregurgitatie, bacteriële endocarditis,
tromboëmbolisme en voorkamerfibrillatie zijn weinig frequent en bij slechts 3%
van de patiënten aanwezig. De meest voorkomende etiologie van systolische
mitralisklepregurgitatie bij patiënten die worden doorverwezen voor chirurgie
blijft de myxomateuze degeneratie (29-70% van de gevallen).
HISTOPATHOLOGIE3
De belangrijkste histologische kenmerken zijn een proliferatie van de
spongiosa van de klepbladen en de vervanging van het klepbladcollageen door
mucopolysaccharidezuur. Hierdoor treden fibrose van de oppervlakte van de
klepbladen, verdunning en/of elongatie van de chordae tendineae en ventriculaire
frictie laesies op. De chordae ruptureren eventueel, wat dan nog meer
regurgitatie geeft. Hoewel de grote meerderheid van de individuen zich
presenteert met een klassieke floppy myxomateuze klep, hebben sommige patiënten
een atypische vorm van de ziekte. Bijna 40% van de chirurgische kandidaten heeft
een fibreuze dysplasie van de mitralisklep, een afgezwakte vorm van een floppy
mitralisklep gekarakteriseerd door dunne, bijna doorschijnende klepbladen.
BEHANDELING10-11
Hoewel cardiale symptomen zoals aritmieën en gevolgen van regurgitatie soms
behandeld kunnen worden met medicatie, is de enige manier tot herstel van de
klepbladen een chirurgische ingreep. De voor- en nadelen van een dergelijke
ingreep moeten echter goed tegen elkaar worden afgewogen. Observatie van de
patiënt met ernstige mitralisklepregurgitatie anticiperend op de ontwikkeling
van ernstige symptomen, leidt tot een hoge incidentie van postoperatieve
complicaties en een slechtere overleving op lange termijn. Daarentegen worden de
beste chirurgische resultaten bekomen bij patiënten met weinig tot geen
symptomen en geen tekens van linker ventriculaire dysfunctie. Uit een studie is
gebleken dat in geval van een klepreparatie de tienjaarsoverleving 68 ± 6% was,
tegen 52 ± 4% voor patiënten die een klepvervanging ondergingen10.
GENETICA
Mitralisklepprolaps kan sporadisch of familiaal zijn, zowel autosomaal dominant
als X-gebonden. Men heeft reeds verschillende loci gevonden op de chromosomen
16, 11 en 13 die gelinkt worden aan mitralisklepprolaps. Familiale genetische
linkage studies werden uitgevoerd om de loci voor mitralisklepprolaps te mappen.
In 1999 werd de eerste locus gemapt op chromosoom 16p11,2-p12,120. De
maximale LOD-score was 5,6. Doorbraken in recombinatietechniek beschreven een
regio van bijna 5 mb, maar een specifieke mutatie verantwoordelijk voor de
ziekte werd niet gevonden. Enkele jaren later werd een tweede locus voor
mitralisklepprolaps gemapt op chromosoom 11p15,421, waarvan men
aannam dat dit een autosomaal dominante ziekte met leeftijdsafhankelijke
penetrantie betrof. Een derde chromosomale locus voor mitralisklepprolaps werd
gemapt op chromosoom 13q31,3-q32,122 met een LOD-score van 3,17. Het
haplotype betrof een chromosomaal segment van meer dan 8 mb.
Voor een vierde locus, die gelegen is op chromosoom X en al in 1969 werd ontdekt23,
is het gelukt om een mutatie in het filamine A gen te vinden. De betreffende
missense mutaties zijn G288R, P637Q, en V711D. Zij veroorzaken verandering in de
eiwitsynthese en daarmee een polariteitsverandering die de eiwitfunctie
verstoort. Filamine A dient ter inhibitie van Smad, een TNF-β inhbitor. Het is
een fosfoproteïne dat actinefilamenten kruiselings verbindt en het actine
cytoskelet aan het plasmamembraan bindt door interactie met actine en
membraanproteïnes zoals β-integrines. Filamine bestaat uit een actinebindend
domein aan de N-terminus en 24 homologe repeats die de ruggengraat van het
proteïne vormen. Iedere repeat bestaat uit 7 antiparallelle β-ketens die in 2
β-vlakken gerangschikt zijn. Filamines bestaan in vivo als dimeren gemedieerd
door interacties tussen de C-terminale sequenties. Uit het onderzoek is tevens
gebleken dat deze mutatie niet alleen mitralisklepprolaps kan veroorzaken, maar
ook van invloed kan zijn op de andere hartkleppen.
LEVENSKWALITEIT24
Er is een onderzoek gedaan naar de gezondheidsgerelateerde levenskwaliteit van
kinderen met mitralisklepprolaps en de impact van de klinische symptomen hier
op. Met behulp van een vragenlijst die het fysiek welbevinden, het psychologisch
welbevinden, autonomie en ouders, vrienden en sociale ondersteuning en school in
kaart brengt, werd vooral daling gevonden van gezondheid en eigen fysieke
activiteit. De resterende bestudeerde dimensies van levenskwaliteit bleken
vergelijkbaar met gezonde kinderen. Binnen de populatie van kinderen die lijden
aan mitralisklepprolaps heeft de frequentie van klinische symptomen echter ook
effect op de verschillende dimensies van levenskwaliteit.

 Het
mitralisklepsysteem (figuur 1.) bestaat uit vier delen en vormt de poort tussen
linker atrium en ventrikel. In een functioneel samenspel met de twee voornoemden
vormen annulus, twee klepbladen (figuur 2), chordae tendineae en
papillairspieren samen een complex dat bepalend is voor de sufficiëntie van de
gehele mitralisklep1,2.
Het
mitralisklepsysteem (figuur 1.) bestaat uit vier delen en vormt de poort tussen
linker atrium en ventrikel. In een functioneel samenspel met de twee voornoemden
vormen annulus, twee klepbladen (figuur 2), chordae tendineae en
papillairspieren samen een complex dat bepalend is voor de sufficiëntie van de
gehele mitralisklep1,2. 




